Neuronale Verarbeitung von Geruchsreizen im Riechkolben der Maus
Forschungsbericht (importiert) 2010 - Max Planck Institut für medizinische Forschung
Jede Sekunde prasseln überall unzählige Sinneseindrücke auf uns ein – seien es beispielsweise die Stimmen von Menschen, die uns am Hauptbahnhof umgeben, während Gerüche von Gebäck und Kaffee mit dem Gestank heranfahrender Züge wetteifern, seien es Tierstimmen und Blätterrauschen in der freien Natur. Wie sind wir in der Lage, all diese Eindrücke voneinander zu trennen, sie zu verarbeiten, eine Stimme von einer anderen zu unterscheiden oder auch nur das Gesicht eines Bekannten aus der Menge heraus zu erkennen? Welche Mechanismen im Gehirn, welche Verschaltungen zwischen Nervenzellen dem zugrunde liegen, ist eine zentrale Frage der Neurowissenschaften.
Vom Reiz zum Verhalten – die Geschwindigkeit der Geruchsverarbeitung
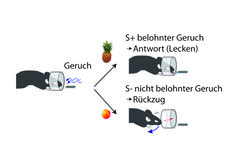
Das olfaktorische System, die neuronale Verarbeitung von Gerüchen, bietet als Modellsystem zahlreiche Vorteile: Der Geruchssinn ist für viele Tiere, insbesondere nachtaktive Tiere, ein zentraler Sinn, sodass Verhaltensuntersuchungen an dem für genetische Methoden besonders gut geeigneten Säugetiermodell – der Maus – möglich werden. Dies erlaubte zum Beispiel, in computergestützten Konditionierungsexperimenten direkt die Zeit zu messen, die für die Geruchsverarbeitung notwendig ist, und so einen Rahmen für die mechanistische Untersuchung der Nervenzell-Netzwerke zu stecken (Abb. 1). Diese Experimente zeigten, dass schon nach weniger als 250 Millisekunden eine perfekte Unterscheidung zweier verschiedener Gerüche (im gezeigten Beispiel monomolekulare Geruchsstoffe, Amylacetat [bananenartig] und Buttersäureethylester [ananasartig]) möglich ist [1; 2]. Erst wenn die beiden verwendeten Gerüche deutlich ähnlicher werden (zum Beispiel Mischungen der genannten Substanzen mit ähnlichem Mischungsverhältnis: 40% A und 60% B verglichen mit 60% A und 40% B), können Mäuse die beiden Mischungen zwar noch sicher unterscheiden, benötigen dafür aber deutlich länger – etwa 70-100 Millisekunden. Diese Experimente zeigten also zunächst eine überraschend schnelle Geruchsverarbeitung. Des Weiteren warfen sie unmittelbar die Frage auf, was in der zusätzlich benötigten Zeit im Gehirn der Mäuse geschieht, damit auch sehr ähnliche Mischungen tatsächlich unterschieden werden können.
Aufbau des Geruchssystems der Maus
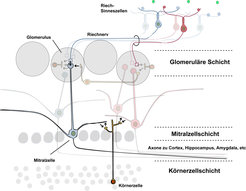
Bei dem Versuch, diese Frage zu beantworten, wird ein weiterer Vorteil des Geruchssystems als Modellsystem offenkundig: Der anatomische Aufbau ist, zumindest aus makroskopischer Sicht, vergleichsweise überschaubar (Abb. 2), [3]. Die Sinneszellen im Nasenepithel wandeln an ihren spezialisierten Nervenendigungen, die in die Nasenschleimhaut hineinragen, chemische Signale – Geruchsstoffe – in elektrische Signale um. Die Axone der Sinneszellen reichen dann direkt in den Riechkolben (bulbus olfactorius) hinein, eine bei Mäusen und vielen anderen Tieren ausgesprochen distinkte und ausgeprägte Struktur im Vorderhirn. Dort bilden die Axone der Rezeptorneuronen direkt synaptische Kontakte mit den Projektionsneuronen des bulbus olfactorius, den sogenannten Mitralzellen. Diese wiederum projizieren in eine Vielzahl kortikaler und subkortikaler Hirnstrukturen, unter anderem in den Hippocampus, der mit Gedächtnisleistungen in Verbindung gebracht wird, oder in den Mandelkern (Amygdala), der in der Angstverarbeitung eine große Rolle spielt.Dies legt die Vermutung nahe, dass Mechanismen der spezifisch olfaktorischen Signalverarbeitung zu einem wesentlichen Teil im bulbus olfactorius verortet sind. In diesem wiederum wird nach heutigem Wissensstand die Verarbeitung von hemmenden Verbindungen dominiert, die von den in großer Zahl vorhandenen Körnerzellen vermittelt wird (Abb. 2). Diese anatomischen Betrachtungen erlauben daher die Spekulation, dass die zur Verarbeitung ähnlicher Gerüche notwendige zusätzliche Zeit möglicherweise zumindest zum Teil auf Vorgänge in diesem inhibitorischen Netzwerk zurückzuführen ist.
Gezielte genetische Veränderungen des bulbus olfactorius
Um dieser Hypothese nachzugehen, wird es notwendig, eine gezielte Veränderung des Körnerzell-Netzwerkes vorzunehmen und die Konsequenz einer solchen Veränderung durch die verschiedenen Beschreibungsebenen – Zelle, Netzwerk, Verhalten – analytisch zu verfolgen. Die vielleicht größte Herausforderung dabei ist es, den Eingriff auf einen definierten, abgegrenzten Raum zu beschränken. Dies ist notwendig, um ausschließlich das genannte Körnerzell-Netzwerk zu verändern, ohne solche Hirnareale zu stören, die zum Beispiel für die Ausführung der Bewegungsabläufe oder den generellen Entscheidungsprozess von Bedeutung sind. Genetische Veränderungen – zum Beispiel das gezielte „Ausknocken” einzelner Gene – manipulieren im Allgemeinen jedoch Zielgene in jeder Körperzelle. Moderne genetische Techniken erlauben es nun, gezielt ein einzelnes Gen mit speziellen Schnittstellen, sogenannten loxP-Stellen, zu flankieren [4]. Wird dann Cre-Rekombinase, ein aus Bakteriophagen stammendes Enzym, in einer Zelle exprimiert, so wirkt diese Rekombinase wie eine molekulare Schere, die das Gen an den loxP-Stellen irreversibel herausschneidet. Durch eine Beschränkung der Expression von Cre-Rekombinase auf Gruppen von Neuronen können somit im Prinzip genetische Veränderungen auf eben diese Gruppen von Neuronen beschränkt werden.
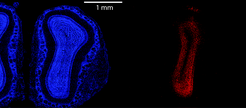
Um dies auf die Körnerzellen des bulbus olfactorius anzuwenden, müssen Viren, die als Genfähren die Information zur Herstellung von Cre-Rekombinase tragen, gezielt durch stereotaktische Injektionen in das Zentrum des bulbus olfactorius eingebracht werden (Abb. 3). Auf diese Weise können beliebige Zielgene spezifisch ausgeschaltet werden – vorausgesetzt es existiert eine Mauslinie, in der das Zielgen von loxP-Schnittstellen flankiert ist.
Bidirektionale Modifikation von Inhibition und Geruchsunterscheidung
Zur Veränderung der inhibitorischen Verschaltung bieten sich speziell Zielgene an, die eine Bedeutung in der synaptischen Übertragung von Mitralzellen auf Körnerzellen haben. In Zusammenarbeit mit Peter Seeburg, Rolf Sprengel, Thomas Kuner und Veronika Egger konnte dabei gezeigt werden, dass – wie aus anderen Hirnregionen bekannt – eine Entfernung des GluA2-Rezeptors zu vermehrtem Einstrom von Kalziumionen in Körnerzellen führt [5]. Dieser wiederum bedingt einen deutlichen Anstieg der Inhibition auf Mitralzellen. Untersucht man auf diese Art gezielt genetisch veränderte Mäuse auf ihre Fähigkeit, Gerüche zu unterscheiden, so kann man feststellen, dass Geruchslernen und -Gedächtnis sich nicht von Kontrollgruppen unterscheiden und sich auch in allgemeinen Verhaltentests aufgrund der sehr regionalen Veränderung keine Unterschiede zeigen.
Bei der Messung der Verarbeitungsgeschwindigkeit waren allerdings deutliche Veränderungen sichtbar: Zwar war die einfache Geruchsunterscheidung ähnlich schnell wie
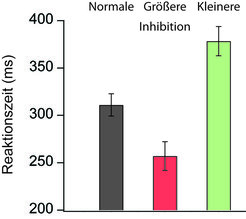
in Kontrolltieren, zur Unterscheidung sehr ähnlicher Geruchsmischungen benötigten die genetisch veränderten Tiere mit erhöhter Inhibition allerdings deutlich weniger Zeit; sie waren schneller als ihre Kontrollartgenossen im selben Experiment (Abb. 4)! Eine analoge Modifikation des GluN1-Rezeptors, die zu geringerem Kalziumeinstrom und geringerer Inhibition führte, zeigte den genau gegenteiligen Effekt: Bei unveränderter Lern- und Gedächtnisleistung benötigte die Unterscheidung ähnlicher Gerüche signifikant mehr Zeit.
Zusammen mit weiteren physiologischen und Verhaltensexperimenten an genetisch veränderten Tieren [6] zeigen diese Versuche, dass das inhibitorische Netzwerk des bulbus olfactorius in der Tat von wesentlicher Bedeutung in der Geruchsprozessierung ist. Die Frage bleibt, auf welche Weise die hemmende Verschaltung Geruchsverarbeitung optimieren kann. Erste physiologische Messungen von einzelnen Mitralzellen im bulbus olfactorius legen nahe, dass Inhibition eine Diversifizierung der Reizantworten ermöglicht. Pharmakologische und optogenetische Manipulationen und eine genaue Untersuchung der verschiedenen Zellpopulationen des bulbus olfactorius werden nun zeigen müssen, welche Aspekte der Geruchskodierung diese Diversifizierung verbessert, und auf welche Weise Nervenzell-Netzwerke der Flut an Sinneseindrücken Herr werden können



