Lebererkrankungen
Viele Lebererkrankungen führen zur Bildung einer Fibrose, die letztendlich eine Zirrhose und Leberversagen verursacht. Die Fibrose ist Folge der Ansammlung von Molekülen der extrazellulären Matrix inkl. Fibronektin und Kollegen Typ I. Diese Moleküle werden u.a. von den Sternzellen der Leber produziert, wenn sie mit dem Zytokin TGF-b stimuliert werden.
Unsere Gruppe zeigte erstmals, dass die Isoformen des Fibronektins erhöht sind bei Patienten mit chronisch cholestatischen Lebererkrankungen. Die Beteiligung einer Isoform des Fibronektins (nämlich der onkofötalen Isoform) bei der assoziierten sekundären Osteoporose konnte ebenfalls festgestellt werden (Kawelke et al. https://www.biochem.mpg.de/en/rg/nakchbandi/publications) (siehe unten unter Osteoporose). Des Weiteren konnten wir bestätigen, dass bei einem Drittel der Patienten mit chronischer Hepatitis C Infektion das Ausmaß der entstehenden Fibrose vorhergesagt werden kann, da bei diesen Patienten die Fibronektin-Isoformen beeinträchtigt sind (Hackl et al. https://www.biochem.mpg.de/en/rg/nakchbandi/publications).
Basierend auf diesen Arbeiten haben wir damit begonnen, die Auswirkungen einer Ausschaltung des Fibronektins in den Sternzellen zu untersuchen. Da ein vollständiger Fibronektin-Knockout bereits in utero letal ist, musste dies mittels des Cre-loxP Systems erfolgen. In diesem System wird das Fibronektin-Gen mit zwei sogenannten loxP Stellen jeweils oberhalb und unterhalb des ATG-Startkodons versehen. Zellen, deren Fibronektin-Gen ausgeschaltet werden soll, wird die Cre-Rekombinase unter der Kontrolle eines Promoters inseriert, welcher spezifisch in dem zu untersuchenden Zelltypen aktiviert wird. Die Cre-Rekombinase ist dann in der Lage, das Gen an den loxP Stellen zu schneiden und die Schnittstellen wieder miteinander zu verbinden. Dies führt zu einem defekten Gen und letztendlich zum Verlust des Fibronektins.
Mäuse, die nicht dazu in der Lage waren, in den Sternzellen Fibronektin zu produzieren, zeigten schon unstimuliert eine deutliche Verstärkung der Fibrosebildung, was zunächst sehr überraschend war (Abbildung). Daraus lässt sich schließen, dass die Sternzellen in Abwesenheit von Fibronektin überstimuliert sind. Wir gehen davon aus, dass die TGF-b Produktion, bzw. Speicherung Fibronektin benötigt (Kawelke et al. Link: https://www.ncbi.nlm.nih.gov/pubmed/22140539).
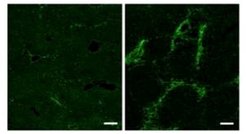
Weitere Arbeiten auf diesem Gebiet beinhalten die Untersuchung der Fibrosebildung bei Mäusen, bei denen Fibronektin in mutierter Form produziert wird und daher nicht mit RGD-bindenden Integrinen interagieren kann. Auch untersuchen wir, wie man die Matrixansammlung, und somit die Fibrose vermindern kann. Ergebnisse dazu wurden bereits publiziert (Altrock et al. Link: http://www.sciencedirect.com/science/article/pii/S016882781400405X?via%3Dihub).
